Artículos originales
Validación de la cuantificación de interleucina 6 en líquido amniótico con utilidad predictiva en el parto pretérmino espontáneo
Validation of interleukin 6 quantification in amniotic fluid with predictive utility in spontaneous preterm delivery
Validación de la cuantificación de interleucina 6 en líquido amniótico con utilidad predictiva en el parto pretérmino espontáneo
Bioquímica y Patología Clínica, vol. 89, núm. 2, pp. 24-30, 2025
Asociación Bioquímica Argentina
Resumen: Introducción: La inflamación intraamniótica se evidencia en la elevación de citocinas y quimiocinas proinflamatorias, entre ellas, la interleucina 6, aun en ausencia de infección de la placenta. Ambas situaciones generan una disminución de la latencia del parto, con altas tasas de morbimortalidad perinatal. Debido a las consecuencias deletéreas inherentes al parto pretérmino, se han propuesto marcadores bioquímicos para evaluar su riesgo, como es la determinación de interleucina 6 en líquido amniótico. Objetivos: Validar la cuantificación de interleucina 6 en líquido amniótico de mujeres embarazadas sanas a las que se les practicó una cesárea en un hospital universitario de comunidad durante los meses de mayo a octubre de 2021. Materiales y métodos: Se realizó un estudio prospectivo a partir de un análisis de precisión y veracidad (EP15-A3), linealidad (EP6-A) e intervalos de referencia (EP28-A3C). Las muestras utilizadas se obtuvieron a partir de la reconstitución de controles comerciales con líquido amniótico. Resultados: La interleucina 6 en líquido amniótico tuvo una performance intra e interensayo ≤2,5 %. La veracidad fue validada desde el punto de vista clínico con un sesgo máximo obtenido de 5 %. El método es estadísticamente lineal en el rango de 1,5 a 4052 pg/ml. Y, por último, se obtuvo un intervalo de referencia de 81 a 1714 pg/ml. Conclusiones: Se logró realizar una validación en una matriz distinta a la ensayada por el fabricante, en este caso, la interleucina 6 en líquido amniótico, con el fin de ser utilizada en un modelo de predicción multivariable.
Palabras clave: interleucina 6, líquido amniótico, trabajo de parto prematuro, estudio de validación, matriz alternativa, validación analítica alternativa.
Abstract: Introduction: Intra-amniotic inflammation is evidenced by the increase in proinflammatory cytokines and chemokines, including interleukin 6, even in the absence of infection of the placenta. Both situations generate a decrease in the time between the onset of contractions and delivery, with high rates of perinatal morbidity and mortality. Due to the inherent deleterious consequences of preterm delivery, biochemical markers, such as the determination of interleukin 6 in amniotic fluid, have been proposed to assess its risk. Aims: To validate the quantification of interleukin 6 in amniotic fluid of healthy pregnant women who underwent a Cesarean section in a Community University Hospital between May and October 2021. Materials and methods: The study was a prospective study based on the analysis of precision and trueness (EP15-A3), linearity (EP6-A) and reference intervals (EP28-A3C). The samples used were obtained from the reconstitution of commercial controls with amniotic fluid. Results: Interleukin 6 in amniotic fluid had an intra- and inter-assay performance ≤ 2.5 %. Trueness was validated from the clinical point of view and a maximum bias of 5 % was obtained. The method was statistically linear in the range from 1.5 to 4052 pg/mL. Finally, a reference interval of 81 to 1714 pg/mL was obtained. Conclusions: It was possible to carry out a validation in a matrix other than the one tested by the manufacturer, in this case, interleukin 6 in amniotic fluid, to be used in a multivariable prediction model.
Keywords: interleukin 6, amniotic fluid, obstetric labor, premature, validation study, alternative matrix, alternative analytical validation.
Introducción
Según el Colegio Americano de Obstetras y Ginecólogos, el parto pretérmino se define como aquel que ocurre antes de la semana 371,2. Esta condición se constituye como la principal causa de muerte perinatal y de secuelas a corto y largo plazo del sobreviviente debido a la inmadurez de los diferentes órganos, especialmente los pulmones y el sistema nervioso central3.
Entre el 70 y el 80 % de los partos pretérmino ocurren de manera espontánea y resultan del trabajo de parto pretérmino con membranas intactas (40 - 50 %) o de la ruptura pretérmino de las membranas fetales (20 - 30 %)4. Aproximadamente el 25 % restante corresponde al parto médicamente indicado y es resultado de la inducción del parto o la ejecución de una cesárea porque, en el caso de que el embarazo continuara, los trastornos obstétricos que desencadenaron dicha situación exacerbarían el riesgo de vida para la madre, el feto o ambos3.
La inflamación solía asociarse con complicaciones durante el embarazo, como aborto, parto pretérmino y preeclampsia. Sin embargo, actualmente, se considera que el estado proinflamatorio juega un rol fundamental en los embarazos saludables, dado que permite la implantación del blastocisto en el útero y el desencadenamiento del trabajo de parto para el posterior nacimiento del neonato. Por consiguiente, la gestación consiste en una alternancia entre el estado proinflamatorio y antiinflamatorio (o de inmunotolerancia) que favorece el adecuado desarrollo fetal5. Si bien la transición proinflamatoria hacia el final de la gestación ocurre de manera fisiológica, ciertos estímulos pueden ocasionar una transición prematura favoreciendo el trabajo de parto pretérmino y desencadenando, finalmente, el parto en pacientes con las membranas fetales intactas6. Entre estos estímulos, se destacan la invasión microbiana de la cavidad amniótica y/o la inflamación intraamniótica2. Esta última se evidencia en la elevación de citocinas y quimiocinas proinflamatorias, entre ellas, la interleucina 6 (IL-6), las cuales se pueden observar aun en ausencia de infección de la placenta7,8,9,10.
Actualmente, existe un modelo propuesto por Cobo y col.8, que sirve para clasificar a las pacientes embarazadas con amenaza de parto prematuro antes de las 34 semanas, de acuerdo con el riesgo de nacimiento dentro de los 7 días desde la admisión. Esta clasificación permite que quienes pertenezcan al grupo de alto riesgo sean trasladadas a unidades con capacidad de cuidados intensivos neonatales y reciban los tratamientos farmacológicos necesarios para mitigar las consecuencias deletéreas del parto pretérmino. Asimismo, el manejo de las pacientes con bajo riesgo podría modificarse debido al descenso en la intensidad de la intervención farmacológica. Este modelo incluye los siguientes parámetros: edad gestacional de la paciente al momento de la admisión, medición de la longitud cervical y concentración de glucosa e IL-6 en líquido amniótico8,11.
Múltiples marcadores bioquímicos y sus combinaciones orientan sobre el riesgo de parto pretérmino o alertan sobre la presencia de una infección o un estado inflamatorio. Entre los marcadores que evalúan el estado inflamatorio, se destaca la proteína C reactiva y su cuantificación en sangre materna. Si bien valora la vía inflamatoria, este marcador es notoriamente inespecífico y podría verse alterado por otras condiciones12,13,14. Por otro lado, el recuento de glóbulos blancos y la concentración de glucosa en el líquido amniótico dan indicio de infección intrauterina, la cual desencadenaría el parto prematuramente15,16. Cuando la paciente embarazada manifiesta una infección intrauterina, la concentración de IL-6 aumenta rápida y notablemente en el líquido amniótico y se asocia de manera notoria con el riesgo de parto pretérmino espontáneo en pacientes embarazadas asintomáticas15. Esto se debe a la activación de múltiples vías de señalización de la inmunidad innata que estimulan la liberación de ciertas citoquinas, como la IL-617. Su aumento significativo se observa entre 24 y 48 horas antes que se manifiesten los síntomas de una corioamnionitis, infección de la placenta y el líquido amniótico, y dentro de las 72 horas que preceden el nacimiento espontáneo13. Si bien es un marcador extremadamente sensible para detectar la presencia de una infección intraamniótica, la IL-6 también se eleva en casos de inflamación intraamniótica con ausencia de aislamiento de microorganismos en medios de cultivo. Por consiguiente, la determinación de este analito podría revelar la presencia de microorganismos resistentes al aislamiento en medios de cultivo, infecciones en tejidos diferentes del líquido amniótico e incluso, verdaderos estímulos no infecciosos, como un trauma o el desprendimiento de la placenta7.
Por consiguiente, teniendo en cuenta la utilidad de implementar este modelo de predicción y la necesidad de contar con el valor de IL-6, es el objetivo de este trabajo validar la cuantificación de IL-6 en líquido amniótico de mujeres embarazadas sanas, sin ningún factor de riesgo según revisión del equipo médico, a las que se le practicó una cesárea en un hospital universitario de comunidad durante los meses de mayo a octubre de 2021.
Materiales y métodos
Metodología
Se llevó a cabo un eEstudio de validación del ensayo de electroquimioluminiscencia (ECLIA) de tipo sándwich para Elecsys IL-6 en el inmunoanalizador Cobas e601, desarrollado por la empresa Roche Diagnostics. Esta prueba inmunológica detecta de forma cuantitativa la IL-6 en muestras de suero y plasma con un intervalo de medición que va de 1,50 a 5000 pg/ml, por lo cual se debe llevar a cabo una validación, dado que su medición en líquido amniótico supone una modificación de las instrucciones del fabricante, según la norma ISO 15189.
Materiales utilizados
Las muestras empleadas para la evaluación de precisión y veracidad se obtuvieron a partir de los dos niveles de control PreciControl Multimarker y del nivel más alto del calibrador IL-6 CalSet, reconstituidos con muestras de líquido amniótico extraídas por punción del saco amniótico de pacientes embarazadas sanas a las que se les practicó una cesárea. Como criterio de inclusión, se utilizaron muestras de mujeres mayores de 18 años con parto a término y sin ningún factor de riesgo, según revisión del equipo médico.
Ensayos realizados
a) Precisión y veracidad: Con el objeto de verificar la precisión y veracidad del método, se utilizó la guía EP15-A3 User Verification of Precision and Estimation of Bias del Clinical and Laboratory Standards Institute (CLSI). Los datos fueron analizados con el programa GMonitor v8.2.
Repetibilidad: El ensayo se realizó mediante comparación del CVR (coeficiente de variación intracorrida) propio del ensayo con el CVea (coeficiente de variación obtenido por el estado del arte) y UVLR (expansión del valor aceptado). Se utilizó como criterio de aceptación CVR menor que CVea o, de no cumplirse, CVR menor que UVLR.
Precisión intermedia: El ensayo se realizó mediante comparación del CVWL (coeficiente de variación intermedia) con el CVea y UVLWL (expansión del valor aceptado). Se utilizó como criterio de aceptación CVWL menor que CVea o, de no cumplirse, CVWL menor que UVLWL.
Veracidad estadística: Durante 5 días, se realizaron las determinaciones del analito por quintuplicado y se obtuvo su media. Los valores extremos, superior e inferior, se obtuvieron aplicando el test de Student (t). Se utilizó como criterio de aceptación que la media obtenida estuviera comprendida dentro del rango definido por los valores inferior y superior.
Veracidad clínica: El ensayo se realizó comparando el ESa(c) (error sistemático aceptable en unidades de concentración) con el sesgo (también en unidades de concentración). Se utilizó como criterio de aceptación que el sesgo fuera menor que el Esa, que se define como el 50 % del ETa (error total aceptable).
b) Linealidad: Para el ensayo de linealidad se utilizó una muestra de líquido amniótico con concentración elevada de IL-6, proveniente de una paciente con parto pretérmino, a partir de la cual se realizaron 5 diluciones equidistantes con el diluyente universal del laboratorio Roche. Se procesaron las muestras por duplicado.
La guía Evaluation of the Linearity of Quantitative Analytical Methods (EP6-A) propuesta por el CLSI fue empleada para la validación del requisito de linealidad. El procesamiento de los datos se efectuó con el software LinChecker.
c) Intervalo de referencia: Para realizar este estudio, se requirieron 120 muestras de líquido amniótico extraídas por punción del saco amniótico de pacientes embarazadas sanas a las que se les practicó una cesárea.
Se procedió de acuerdo con la guía del CLSI EP28-A3C Defining, Establishing, and Verifying Reference Intervals in the Clinical Laboratory con el objeto de evaluar los límites de referencia. Los datos obtenidos fueron analizados con el software EP Evaluator 12.3.0.2.
Requerimientos de calidad
Los coeficientes de variación utilizados no corresponden a los parámetros estadísticos provistos por el fabricante, sino a valores determinados que se asignan, ya que se trata de una técnica sin controles comerciales. Se definió como criterio de aceptabilidad el CVea de 2 % para los tres niveles ensayados. Dicho valor corresponde al menor coeficiente de variación obtenido de los controles comerciales utilizados para IL-6 en suero durante el mes que se llevó a cabo el procesamiento del ensayo de precisión. Incluso este valor es menor que los brindados por el fabricante para los controles comerciales de IL-6 en suero.
El ETa utilizado es 15 %, el cual se determinó mediante el método del estado del arte18. El valor se obtuvo mediante el cálculo ETa%=CVp*3, donde CVp es el coeficiente de variación ponderado, obtenido a partir de los controles de IL-6 en suero durante el año 2021, calculado de acuerdo con la siguiente fórmula: CVp=∑(Nm. CVm)/∑Nm, donde Nm es la cantidad de controles que se corrieron durante un mes y CVm es el coeficiente de variación mensual correspondiente a dicho mes.
Resultados
a) Precisión y veracidad. Repetibiliad: De los tres niveles evaluados, los dos primeros se aceptaron, ya que los valores obtenidos de CVR propios son menores que el requisito objetivo (CVea) de 2 %, en cambio, el nivel 3 se acepta utilizando la expansión del nivel permitido (UVLR). Ver Tabla I.
Precisión Intermedia: De los tres niveles evaluados, los dos primeros se aceptan, ya que los valores obtenidos de CVWL propios son menores que el requisito planteado (CVea) de 2 %, en cambio, el nivel 3 se acepta utilizando la expansión del nivel permitido (UVLWL). Ver Tabla I.
Veracidad estadística: A partir de los datos obtenidos de los distintos niveles ensayados, se calcula la media de las 25 repeticiones para cada uno de los 3 niveles.
Como las medias de los tres niveles se hallan por fuera de los intervalos de medición calculados, la validación es rechazada desde un punto de vista estadístico. Ver Tabla II.
Veracidad clínica: Se evalúa la veracidad clínica por medio de la estimación del sesgo para luego compararlo con el error sistemático permitido. La veracidad es verificada desde el punto de vista clínico, puesto que el sesgo es inferior al 50 % del ETa. Ver Tabla III.
b) Linealidad: El análisis de los datos y la consiguiente obtención de la ecuación de la recta permiten establecer la ausencia del error de no linealidad; por tanto, se verifica que el método es estadísticamente lineal en el rango de concentraciones evaluado, siendo el mismo de 1,5 a 4052 pg/ml. Ver Tabla IV y Figura 1.
c) Intervalo de referencia: Se obtuvo un rango de referencia de 81 a 1714 pg/ml (expresado en log10: de 1,9 a 3,2). Ver Tabla V.
| Repetibilidad | Precisión intermedia | |||||
| Nivel | CVR | CVea | UVLR | CVWL | CVea | UVLWL |
| 1 | 1,0 | 2,0 | 2,7 | 1,1 | 2,0 | 2,6 |
| 2 | 1,1 | 2,0 | 2,7 | 1,2 | 2,0 | 2,6 |
| 3 | 2,5 | 2,0 | 2,7 | 2,5 | 2,0 | 2,6 |
| Nivel | |||
| 1 | 2 | 3 | |
| Valor evaluado (pg/ml) | 246,0 | 454,5 | 867,4 |
| Media (pg/ml) | 237,2 | 431,7 | 830,9 |
| Valor Inferior (pg/ml) | 243,7 | 450,1 | 850,8 |
| Valor superior (pg/ml) | 248,3 | 458,9 | 883,9 |
| Nivel | |||
| 1 | 2 | 3 | |
| ESa (c) (pg/ml) | 18,5 | 34,1 | 65,1 |
| Sesgo (c) (pg/ml) | -8,8 | -22,8 | -36,5 |
| Sesgo% | 3,6 | 5,0 | 4,2 |
| Muestra | Valor asignado (pg/ml) | Replicado 1 (pg/ml) | Replicado 2 (pg/ml) |
| 1 | 1,5 | 23,6 | 24,2 |
| 2 | 1014,1 | 1045,0 | 1046,0 |
| 3 | 2026,7 | 2053,0 | 2076,0 |
| 4 | 3039,4 | 3079,0 | 3141,0 |
| 5 | 4052,0 | 3939,0 | 4119,0 |
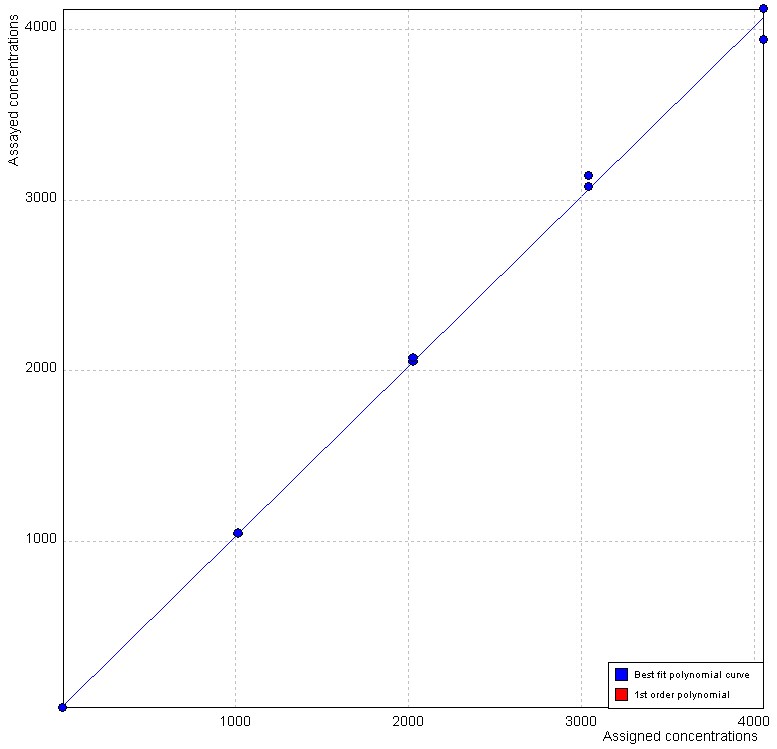
Figura 1.
Rango lineal de IL-6 en líquido amniótico
| Muestra | Resultado (pg/mL) | Muestra | Resultado (pg/mL) | Muestra | Resultado (pg/mL) | Muestra | Resultado (pg/mL) |
| 1 | 311,7 | 31 | 222,9 | 61 | 359,7 | 91 | 540,6 |
| 2 | 1425,0 | 32 | 345,5 | 62 | 151,7 | 92 | 1716,0 |
| 3 | 271,1 | 33 | 517,7 | 63 | 611,3 | 93 | 256,5 |
| 4 | 1185,0 | 34 | 208,5 | 64 | 618,8 | 94 | 350,8 |
| 5 | 286,4 | 35 | 179,5 | 65 | 616,6 | 95 | 340,8 |
| 6 | 595,7 | 36 | 986,9 | 66 | 532,1 | 96 | 580,8 |
| 7 | 1183,0 | 37 | 92,9 | 67 | 471,0 | 97 | 345,8 |
| 8 | 94,8 | 38 | 80,2 | 68 | 377,1 | 98 | 124,2 |
| 9 | 1276,0 | 39 | 123,0 | 69 | 1866,0 | 99 | 396,7 |
| 10 | 1403,0 | 40 | 1376,0 | 70 | 738,6 | 100 | 690,2 |
| 11 | 199,3 | 41 | 456,9 | 71 | 283,3 | 101 | 661,1 |
| 12 | 1544,0 | 42 | 462,1 | 72 | 126,5 | 102 | 194,5 |
| 13 | 182,1 | 43 | 276,5 | 73 | 1238,0 | 103 | 453,3 |
| 14 | 148,7 | 44 | 697,3 | 74 | 234,7 | 104 | 327,5 |
| 15 | 571,8 | 45 | 188,8 | 75 | 939,4 | 105 | 985,8 |
| 16 | 1854,0 | 46 | 197,9 | 76 | 193,0 | 106 | 515,5 |
| 17 | 1044,0 | 47 | 377,9 | 77 | 196,1 | 107 | 328,6 |
| 18 | 537,8 | 48 | 479,7 | 78 | 387,0 | 108 | 189,9 |
| 19 | 652,2 | 49 | 878,7 | 79 | 588,3 | 109 | 220,2 |
| 20 | 270,0 | 50 | 319,3 | 80 | 72,2 | 110 | 71,8 |
| 21 | 502,0 | 51 | 1002,0 | 81 | 228,5 | 111 | 218,4 |
| 22 | 539,8 | 52 | 477,0 | 82 | 627,8 | 112 | 308,4 |
| 23 | 347,4 | 53 | 258,7 | 83 | 241,2 | 113 | 1159,0 |
| 24 | 439,1 | 54 | 724,1 | 84 | 694,1 | 114 | 646,3 |
| 25 | 1650,0 | 55 | 612,4 | 85 | 817,7 | 115 | 305,5 |
| 26 | 453,1 | 56 | 158,9 | 86 | 375,1 | 116 | 697,3 |
| 27 | 307,7 | 57 | 238,0 | 87 | 338,1 | 117 | 151,9 |
| 28 | 265,4 | 58 | 275,4 | 88 | 209,0 | 118 | 197,0 |
| 29 | 229,9 | 59 | 270,0 | 89 | 441,4 | 119 | 312,5 |
| 30 | 1304,0 | 60 | 770,3 | 90 | 1435,0 | 120 | 1040,0 |
Discusión
Con el avance de las investigaciones científicas y la rápida difusión de los resultados, es cada vez más frecuente que se solicite a los laboratorios de análisis clínicos la determinación de analitos en matrices diferentes de las evaluadas inicialmente. Esto implica el desafío de validar marcadores bioquímicos en una nueva matriz para la cual no suele haber controles y calibradores comerciales19. En este sentido, se llevó a cabo la validación de IL-6 en LA a fin de garantizar la calidad de los resultados dando respuesta a una necesidad médica.
La utilidad de esta validación reside en la inclusión de la determinación de IL-6 en LA como parte de un modelo de predicción multivariable que ha demostrado una tasa de detección de parto espontáneo dentro de los 7 días del 87 %, una tasa de falsos positivos del 33 % y un valor predictivo negativo del 80 %, poniendo de manifiesto la eficiencia diagnóstica de este modelo8. Resulta así la IL-6 el analito con la mejor sensibilidad y especificidad en la detección del parto espontáneo en comparación con otros mediadores inflamatorios, y su asociación con la longitud cervical contribuye a la predicción del parto pretérmino espontáneo13.
Una de las ventajas del modelo de predicción desarrollado y validado por Cobo y col. es que comprende variables mensurables inmediatamente luego de la admisión o al cabo de unas horas, incluyendo parámetros clínicos (longitud cervical medida por ultrasonido), epidemiológicos (edad gestacional al momento de la admisión) y bioquímicos (glucosa e IL-6 en el líquido amniótico)8. La validación de la determinación de IL-6 en LA permite completar las variables y, de este modo, aplicar el modelo de predicción a las pacientes de nuestro hospital.
En cuanto a las limitaciones de este trabajo, en primer lugar, los valores de IL-6 en LA esperados en la población objetivo (mujeres con embarazos únicos de menos de 34 semanas, ingresadas con diagnóstico de trabajo de parto prematuro y membranas intactas) se encuentran en el rango de 1020 a 20800 pg/ml, según Cobo y col.8. Sin embargo, para los estudios de precisión y veracidad, en nuestro trabajo, se utilizaron muestras con niveles de IL-6 muy inferiores, determinados por la concentración en los materiales comerciales disponibles. En este mismo sentido, no se consideró necesaria la determinación del límite de cuantificación debido a que los valores esperables en pacientes con riesgo de parto pretérmino son muy superiores al límite inferior del rango analítico (1,5 pg/ml). Asimismo, tampoco se realizó el estudio de estabilidad, ya que esta práctica es considerada de urgencia en nuestro medio, y la relevancia de la información que arroja supone el procesamiento de la muestra de manera inmediata.
Por otro lado, en el presente trabajo, el rango de referencia fue determinado en muestras de pacientes con embarazos a término, mientras que Cobo y col.8 utilizan el modelo de predicción en una población de embarazadas pretérmino. Sin embargo, hay autores que evidenciaron que los niveles de interleucina 6 en el líquido amniótico permanecen relativamente estables durante el embarazo y no se ven afectados por la edad gestacional ni por factores maternos como el origen étnico, edad, índice de masa corporal (IMC), tabaquismo, paridad o método de concepción. Los valores de referencia que se obtuvieron en el presente trabajo, expresados en log10, son semejantes a los obtenidos por Del Barco y col., a pesar de que el análisis haya sido efectuado en semanas de gestación diferentes20,21. Cabe destacar la limitación que representa el tipo de muestra y el modo de obtención, teniendo en cuenta la dificultad de realizar una amniocentesis a pacientes embarazadas de menos de 34 semanas sin trabajo de parto prematuro. Este es justamente un obstáculo importante para la aplicación del modelo aun en pacientes candidatas al mismo. En muchos de los trabajos hasta el momento publicados, se ha dosado IL-6 en muestras que fueron obtenidas con otros objetivos como, por ejemplo, estudios genéticos20,21.
Otro aspecto a considerar es que, al ser una práctica realizada en una matriz no validada por el fabricante, no se cuenta con requisitos de calidad tabulados en las fuentes habitualmente consultadas22, lo que genera la necesidad de utilizar como objetivos de calidad aquellos establecidos según el estado del arte en nuestro laboratorio. De todos modos, si bien corresponden a otra matriz (suero), en todos los casos, se utilizaron aquellos datos más desafiantes para ganar en rigurosidad.
Conclusiones
Finalmente, se logró la puesta a punto de la determinación de IL-6 en LA sorteando la dificultad de una validación sin materiales comerciales ni requerimientos de calidad propios para dicha matriz. No obstante, en el mismo sentido que exponen Loyola y col.19, esto genera a futuro la necesidad de contar con controles de calidad internos y externos con el objetivo de mantener la calidad de los resultados informados.
Referencias bibliográficas
1. American College of Obstetricians and Gynecologists’ Committee on Practice Bulletins-Obstetrics. Practice Bulletin No. 171: Management of Preterm Labor. Obstet Gynecol. 2016;128(4):e155-64, https://doi.org/10.1097/aog.0000000000001711
2. Resnik R, Lockwood CJ, Moore T, Greene MF, Copel J, Silver RM. Creasy & Resnik. Medicina maternofetal: Principios y práctica. Elsevier Health Sciences; 2019. 1408 p.
3. Rodríguez M, González Ramírez VE. Relación de las citoquinas proinflamatorias con la corioamnionitis subclínica y el parto pretérmino. Rev Cubana Adm Salud. 2011; 37(4):562-76.
4. Pasquier JC, Doret M. Les complications et la surveillance pendant la période de latence après une rupture prématurée des membranes avantterme: mise au point. J Gynecol Obstet Biol Reprod. 2008;37(6):568-78, https://doi.org/10.1016/j.jgyn.2007.11.031
5. Mor G, Aldo P, Alvero AB. The unique immunological and microbial aspects of pregnancy. Nat Rev Immunol. 2017;17(8):469-82, https://doi.org/10.1038/nri.2017.64
6. Gomez-Lopez N, StLouis D, Lehr MA, Sanchez-Rodriguez EN, Arenas-Hernandez M. Immune cells in term and preterm labor. Cell Mol Immunol. 2014;11(6):571-81, https://doi.org/10.1038/cmi.2014.46
7. Combs CA, Gravett M, Garite TJ, Hickok DE, Lapidus J, Porreco R, et al. Amniotic fluid infection, inflammation, and colonization in preterm labor with intact membranes. Am J Obstet Gynecol. 2014;210(2):125.e1-125.e15, https://doi.org/10.1016/j.ajog.2013.11.032
8. Cobo T, Aldecoa V, Figueras F, Herranz A, Ferrero S, Izquierdo M, et al. Development and validation of a multivariable prediction model of spontaneous preterm delivery and microbial invasion of the amniotic cavity in women with preterm labor. Am J Obstet Gynecol. 2020;223(3):421.e1-21.e14, https://doi.org/10.1016/j.ajog.2020.02.049
9. Goldenberg RL, Culhane JF, Iams JD, Romero R. Epidemiology and causes of preterm birth. Lancet. 2008;371(9606):75-84, https://doi.org/10.1016/s0140-6736(08)60074-4
10. Wei SQ, Fraser W, Luo ZC. Inflammatory cytokines and spontaneous preterm birth in asymptomatic women: a systematic review. Obstet Gynecol. 2010;116(2 Pt 1):393-401, https://doi.org/10.1097/aog.0b013e3181e6dbc0
11. Son M, Miller ES. Predicting preterm birth: Cervical length and fetal fibronectin. Semin Perinatol. 2017;41(8):445-51, https://doi.org/10.1053/j.semperi.2017.08.002
12. Tsiartas P, Holst RM, Wennerholm UB, Hagberg H, Hougaard DM, Skogstrand K, et al. Prediction of spontaneous preterm delivery in women with threatened preterm labour: a prospective cohort study of multiple proteins in maternal serum. BJOG. 2012;119(7):866-73, https://doi.org/10.1111/j.1471-0528.2012.03328.x
13. Holst RM, Hagberg H, Wennerholm UB, Skogstrand K, Thorsen P, Jacobsson B. Prediction of spontaneous preterm delivery in women with preterm labor: analysis of multiple proteins in amniotic and cervical fluids. Obstet Gynecol. 2009;114(2Pt 1):268-77, https://doi.org/10.1097/aog.0b013e3181ae6a08
14. Glover AV, Manuck TA. Screening for spontaneous preterm birth and resultant therapies to reduce neonatal morbidity and mortality: A review. Semin Fetal Neonatal Med. 2018;23(2):126-32, https://doi.org/10.1016/j.siny.2017.11.007
15. Melekoglu R, Yilmaz E, Ciftci O, Kafadar YT, Celik E. Associations between second-trimester amniotic fluid levels of ADAMTS4, ADAMTS5, IL-6, and TNF-α and spontaneous preterm delivery in singleton pregnancies. J Perinat Med. 2019;47(3):304-10, https://doi.org/10.1515/jpm-2018-0297
16. Tarim E, Bağiş T, Kiliçdağ EB, Sezgin N, Yanik F. Are amniotic fluid C-reactive protein and glucose levels, and white blood cell counts at the time of genetic amniocentesis related with preterm delivery? J Perinat Med. 2005;33(6):524-9, https://doi.org/10.1515/jpm.2005.093
17. Prairie E, Côté F, Tsakpinoglou M, Mina M, Quiniou C, Leimert K, et al. The determinant role of IL-6 in the establishment of inflammation leading to spontaneous preterm birth. Cytokine Growth Factor Rev. 2021;59:118-30, https://doi.org/10.1016/j.cytogfr.2020.12.004
18. Westgard JO, Barry PL. Prácticas Básicas de Control de Calidad: Capacitación en Control de Calidad Estadístico para Laboratorios Clínicos. Westgard Quality Corporation; 2010.
19. Loyola L, Colimodio M J, Furci A, Giménez MI, Nardi MA. Validación de un método analítico para cuantificación de ferritina en líquido cefalorraquídeo. Acta bioquím clín latinoam. 2022;56(2):139-48.
20. Del Barco E, Franco-Jarava C, Vargas M, Maíz N, Arevalo S, Sánchez MÁ, et al. Reference values for interleukin-6 in the amniotic fluid of asymptomatic pregnant women. Acta Obstet Gynecol Scand. 2023;102(4):480-5, https://doi.org/10.1111/aogs.14524
21. Gervasi MT, Romero R, Bracalente G, Erez O, Dong Z, Hassan SS, et al. Midtrimester amniotic fluid concentrations of interleukin-6 and interferon-gamma-inducible protein-10: evidence for heterogeneity of intra-amniotic inflammation and associations with spontaneous early (32 weeks) preterm delivery. J Perinat Med. 2012;40(4):329-43, https://doi.org/10.1515/jpm-2012-0034
22. McDaniel L. Total Allowable Error Table [Internet]. Data Innovations. Disponible en: https://www.datainnovations.com/allowable-total-error-table/
Notas de autor
jesica.rolando@hiba.org.ar
Información adicional
redalyc-journal-id: 651

