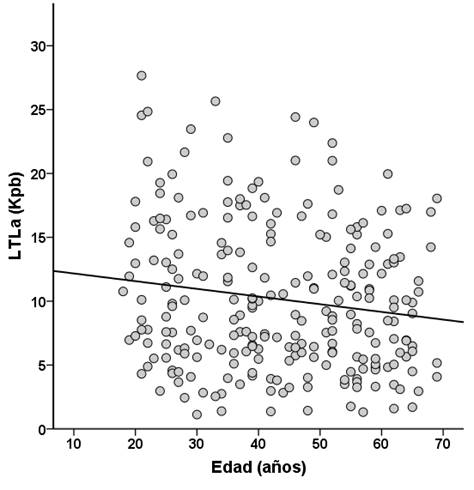
Figura 1. Longitud telomérica leucocitaria absoluta (LTLa) en función de la edad para la población general. Línea de regresión lineal.
Materiales y métodos
Diseño del estudio y poblaciones
Estudio epidemiológico transversal
Se incluyeron en el estudio individuos adultos no relacionados, de ambos sexos, pertenecientes a la población general de Venado Tuerto, provincia de Santa Fe. Fueron reclutados aleatoriamente, entre 2011 y 2017, a través de un diseño de muestreo estratificado, en múltiples etapas .
Se procedió al diagnóstico de SM mediante los criterios del Adult Treatment Panel III (ATP III)34, a partir de la presencia de tres o más de los factores de riesgo cardiometabólico. La presencia de obesidad se determinó a partir del índice de masa corporal (IMC) ≥30 Kgm (-2). Se procedió a la conformación de 3 grupos: uno de individuos con peso normal y sin componentes del SM, que conformó el grupo control, llamado NP0 (NP: normopeso, 0: sin componentes del SM); el segundo grupo, OMS ,(O: obesos, MS: metabólicamente sanos, de acuerdo con el trabajo logrado por un consenso de sociedades médicasinternacionales35) conformado por individuos con obesidad y que presentan hasta 2 de las alteraciones metabólicas características del SM y un tercer grupo de individuos con obesidad y SM, llamado OSM (O: obesos, SM: síndrome metabólico).
Estudios prospectivos controlados
Protocolo de compensación metabólica en individuos con DT2 mediante tratamiento farmacológico y cambios en el estilo de vida
Con el objetivo de analizar los efectos del control metabólico sobre la LTLa a partir de cambios en el estilo de vida, estudiamos un subgrupo de individuos con DT2, antes y después de la intervención con un tratamiento farmacológico y cambios en el estilo de vida. Se incluyeron pacientes con DT2 de reciente diagnóstico y con descontrol metabólico, caracterizado por la determinación de hemoglobina glicosilada (HbA1c) mayor de 8 %, los cuales conformaron el grupo preintervención (0 meses). Estos pacientes recibieron tratamiento farmacológico y medidas higiénico - dietéticas con el fin de lograr la compensación metabólica, demostrada por una disminución en el valor de HbA1c a 7 % o menos. El tratamiento farmacológico incluyó la utilización de drogas antidiabéticas orales, según prescripción médica. Las medidas higiénico - dietéticas incluyeron dieta y ejercicio físico en todos los pacientes. Todos los pacientes fueron reanalizados después de 6 meses de tratamiento y constituyeron el grupo posintervención (6 meses). Todos los participantes dieron su consentimiento informado por escrito y fueron seleccionados de acuerdo con:
Criterios de inclusión: adultos caucásicos no relacionados; de ambos sexos; de 30 a 70 años; nativos argentinos y residentes en zonas urbanas de Buenos Aires; sin antecedentes patológicos personales previos excepto la posible existencia de hipertensión, dislipidemia y/o sobrepeso / obesidad.
Criterios de exclusión: cualquier patología excepto los factores de riesgo cardiovascular mencionados; embarazo; etilismo; drogadicción; antecedentes o sospecha de pancreatitis; consumo reciente de agentes hiperglucemiantes como, por ejemplo, tratamiento con corticoides (<3 meses) e inestabilidad en el peso corporal (pérdida >3 kg en los últimos 12 meses).
Determinación de la LTLa absoluta
La determinación de la LTLa absoluta en muestras de ADN genómico se llevó a cabo por PCR cuantitativa en tiempo real (qPCR) con el método de SYBR ™ Green, como se ha descrito previamente37. Para cada muestra de ADN, se realizó la amplificación por el método de real time en un ciclador Step One de Applied Biosystem, de un fragmento de 75 pb de un GCU (gen de copia única ribosomal, Ribosomal Protein Lateral Stalk Subunit P0, RPLPO) y de las secuencias, teloméricas con primers específicos (RPLPO: Fw: 5’CAGCAAGTGGGAAGGTGT AATCC3’; Rv: 5’CCCATTCTATCATCAACGGGTACAA3’; telómero: Fw 5’CGGTT TGTTTGGGTTTGGGTTTGGGTTTGGGTTTGGGTT3’; Rv: 5’GGCTTGCCTTACCC TTACCCTTACCCTTACCCTTACCCT3’). Ambas PCR se realizaron en un volumen final de 20 µl que contenía 20 ng de DNA, 1X SYBR ™ Green Master Mix y 250 nM de primers para RPLPO o 100 nM para la reacción de telómeros. Las condiciones de PCR fueron: 10 min a 95ºC, seguidos por 45 ciclos de 15 segundos a 95ºC y 1 min a 60ºC. La curva de melting se realizó con 1 ciclo de 20 segundos a 95ºC, 15 segundos a 50ºC y 98ºC con una rampa de temperatura de 0,3ºC/seg. Cada muestra se analizó por duplicado y, en todos los ciclados, se incluyeron estándares de concentración conocida y un control negativo, sin templado, en el que el ADN fue sustituido por agua. Se construyeron curvas de calibración para ambas secuencias a analizar, utilizando cinco diluciones seriadas de oligonucleótidos sintetizados que contienen las repeticiones TTAGGG para las secuencias teloméricas y un oligómero que contiene el producto de RPLP0 para el GCU. Ambas curvas se pusieron a punto hasta obtener una misma eficiencia de la reacción, entre un 90 y 110 %. Para cada muestra en estudio, a partir de la curva de oligonucleótidos de repeticiones TTAGGG, se obtuvo el valor de Kpb/reacción y de la curva del GCU, el número de copias del genoma diploide/reacción. El valor de Kpb/reacción se dividió por el número de copias del genoma (diploide)/reacción para calcular la LTLa en Kpb por genoma diploide humano (relación T/S).
Análisis estadístico
El análisis estadístico se realizó con SPSS Statistics 20.0. Un valor de p inferior a 0,05 fue considerado estadísticamente significativo. La distribución normal de los datos se evaluó mediante la prueba de Shapiro - Wilk. Las comparaciones de las características bioquímicas y clínicas y de la LTLa se realizaron por ANOVA de una vía, seguido de la prueba post hoc de Bonferroni para múltiples factores o grupos y prueba T para muestras relacionadas. Un análisis univariado de ajuste de covarianza (ANCOVA) o regresión lineal múltiple y estudio de variables ficticias permitirá el ajuste por variables confundidoras. La asociación entre LTLa y variables cuantitativas se analizó mediante análisis de correlación parcial. Se utilizó test t para la comparación de datos pareados con el fin de analizar las variaciones en las características bioquímico - clínicas y en la LTLa luego de las intervenciones en individuos con obesidad y DT2.
Resultados
Estudio transversal. Regresión de la LTLa con la edad
Se analizó la relación entre la LTLa y la edad en toda la población, ya que la edad es el principal factor implicado en el acortamiento telomérico. El promedio de la LTLa de la población general fue de 10,18 ± 5,70 kpb. En el análisis, se observó una asociación inversa entre los dos parámetros, edad y LTLa (p = 0,016; B = -0,063; R2 = 0,025 IC del 95% B = -0,115/-0,012) (Figura 1), lo cual demostró que los individuos con edades más avanzadas presentan una menor LTLa. Este dato constituye una medida de validación del método, ya que es un resultado esperado cuando se analiza la LTLa en una población.
Estudio transversal. Caracterización de la población
La población estudiada involucró a 250 individuos: 84 mujeres y 149 hombres (36,1 % y 64,9 %, respectivamente) y una edad media de 43 ± 14 años. El 35,9 % (n = 84) de la población no presentó SM y era normopeso (grupo NP0); 26,5 % (n = 62) de los individuos era metabólicamente sano y presentaba obesidad (grupo OMS) y el 37,6 % (n = 88) presentaba SM y obesidad (grupo OSM). La caracterización bioquímica, clínica y antropométrica de cada grupo se puede observar en la Tabla I.
Estudio transversal. Determinación de la LTLa
La LTLa media fue de 12,40 ± 6,30 kpb para el grupo NP0; de 8,72 ± 4,73 Kpb para el grupo OMS y 9,17 ± 5,22 kpb para los individuos OSM. La LTLa media para el grupo NP0 difiere significativamente de la de los grupos OMS y OSM (p<0,001 en ambos casos). Al analizar el efecto que ejercen los factores de riesgo cardiometabólicos sobre la LTLa, se encontró una asociación significativa entre el mayor número de componentes SM y la menor LTLa (p<0,001; R2 = 0,06, B = -1,275; IC 95% B = -1,926/-0,624), que resistió el ajuste por los factores de edad y sexo (p = 0,004). El estudio post hoc mostró diferencias en particular entre los grupos 0 vs. 1 (p = 0,008); 0 vs. 2 (p = 0,001) y 0 vs. SM (p<0,001). De esta manera, una menor LTLa se asoció a un mayor número de componentes del SM. La presencia de al menos un componente tuvo un impacto negativo sobre la LTLa. No encontramos una asociación significativa entre la LTLa y ninguno de los componentes del SM en particular ni con el IMC, el HOMA o la PCR.
Estudio longitudinal de pacientes con DT2. Caracterización de grupos pre y posintervención.
Se estudiaron 30 individuos con DT2, de los cuales 7 mujeres (26,9 %) y 19 hombres (73,1 %) completaron el protocolo de intervención, con una edad media de 49,35 ± 12,55 años. Las determinaciones bioquímico - clínicas permitieron caracterizar a la población de estudio. Al comparar los grupos pre y posintervención, se encontraron diferencias estadísticamente significativas en los valores de HbA1c (p<0,001) y glucemia (p = 0,001), lo cual demostró una correcta compensación metabólica de los pacientes luego del tratamiento farmacológico y los cambios en el estilo de vida (Tabla II). Además, se observó una disminución en el peso (p = 0,039) e IMC (p = 0,030). El resto de las variables bioquímico - clínicas analizadas no mostró cambios luego de la intervención.
Estudio longitudinal de pacientes con DT2. Determinación de la LTLa
Al evaluar comparativamente la LTLa de los pacientes en los diferentes momentos del estudio, se evidenció un comportamiento aleatorio: en algunos pacientes se observó una disminución de la LTLa luego del tratamiento, en otros se mantuvo y en otros hubo un aumento de la LTLa (Figura 2). Las variaciones en la LTLa no se asociaron al tiempo de tratamiento ni al nivel de compensación metabólica evaluada por la glucemia y la HbA1c. Tampoco se encontró una asociación entre la LTLa de cada momento del tratamiento con ninguna de las variables bioquímico - clínicas analizadas. En cambio, se halló una asociación positiva, significativa entre la variación de la LTLa luego del tratamiento y la dosis de metformina empleada (p = 0,007; R = 0,518; B = 0,003; IC95% B = 0,001/0,005), ya que los individuos que recibieron las mayores dosis de metformina mostraron un aumento en la LTLa.
Estudio longitudinal de pacientes con obesidad. Caracterización de la población
La población total consistió en 22 personas, de las cuales el 54,5 % fueron mujeres (n = 12) y el 45,5 %, hombres (n = 10), con una edad media de 52,91 ± 6,16 años (rango = 41 - 63 años). El abordaje quirúrgico fue por BGYR en el 72,7 % de los casos (n = 16) y por gastrectomía en manga en el 27,3 % (n = 6). En la Tabla III, se muestran las características bioquímico - clínicas y antropométricas de la población en los dos momentos del estudio. Luego de la cirugía bariátrica, se observó una disminución del peso y de los parámetros relacionados con la masa corporal (IMC, nivel de grasa visceral, circunferencia de cintura, contenido de grasa, masa libre de grasa y masa de músculo esquelético). Además, se observó una mejora en los niveles de TG, glucemia y HbA1c. También hubo un aumento significativo en la insulino-sensibilidad demostrado por un descenso del HOMA y una disminución significativa en el nivel de inflamación medido por la PCR-us al mes de la cirugía.
Estudio longitudinal de pacientes con obesidad. Determinación de la LTLa
Se observó una LTLa media significativamente aumentada a los 6 meses de la cirugía en comparación con los niveles basales prequirúrgicos (3,45±1,26 Kpb vs. 5,07±3,10 Kpb, p = 0,013). No se encontró ninguna correlación significativa entre la variación de la LTLa y la ausencia de cambio en las variables bioquímico - clínicas y antropométricas analizadas, así como tampoco, cambios debidos a la presencia de DT2.
Por otro lado, al subdividir a los pacientes por la presencia de obesidad u obesidad mórbida, los pacientes obesos mórbidos, a los 6 meses de la cirugía, presentaron un aumento de la LTLa (3,47±1,47 Kpb a 5,23±2,86 Kpb, p = 0,022), un menor nivel de inflamación medida por PCR us (p = 0,005) y un menor IMC (p<0,001). Los pacientes obesos, por otro lado, si bien disminuyeron significativamente el IMC (p<0,001), no presentaron cambios significativos en la LTLa (3,43±,085 Kpb a 4,78±3,66 Kpb p = 0,287) ni en los niveles de inflamación (p = 0,966). Analizando las variables bioquímicas, clínicas y antropométricas, observamos que los obesos mórbidos que presentaron mayores aumentos en la LTLa son aquellos que mostraron mayores descensos en la PCR como marcador de inflamación (r = - 0,570; p = 0,024) (Figura 3).
Discusión
El SM refiere a una agrupación de factores de riesgo cardiometabólicos que aumenta de 2 a 3 veces el riesgo de desarrollar ECV y 5 veces DT220. Siguiendo los criterios del III Panel de Tratamiento para Adultos (ATP III) del Programa Nacional de Educación sobre el Colesterol (NCEP), se puede identificar de manera precisa y temprana a los individuos con alto riesgo de desarrollar SM y, por lo tanto, se podrían llevar a cabo estrategias para la prevención del desarrollo de dichas enfermedades.
Si bien se usan marcadores biológicos para medir el estado metabólico de un individuo en el momento de la toma de la muestra, utilizamos la LTLa como biomarcador, ya que refleja la carga acumulada del estrés oxidativo y la inflamación que se producen durante el curso de la vida, es decir, la historia metabólica del paciente como precursora de las enfermedades relacionadas con el envejecimiento. Con el aumento de la edad, se ha descripto una pérdida lenta y gradual de la LTLa38,39 como resultado de la incapacidad de la ADN polimerasa de replicar completamente los extremos cromosómicos con cada división celular40,7. Al analizar la relación entre la LTLa y la edad de los pacientes, encontramos una asociación inversa (p= 0,006): los individuos de edades más avanzadas presentaron LTLa más cortas que los individuos más jóvenes. Consistente con nuestros resultados, un estudio sistemático, que incluyó 124 estudios transversales y 5 longitudinales, analizó la asociación de edad con LTLa en leucocitos de individuos adultos y demostró una correlación negativa41.
Además de relacionarse con el envejecimiento fisiológico, el acortamiento telomérico en sangre periférica se ha descripto en pacientes con cáncer42,43, pacientes diabéticos44-48y en individuos con SM y se relacionó con el aumento de los factores de riesgo de ECV49 como el aumento de la presión arterial50, los altos niveles de glucosa en ayunas46.47, obesidad y tabaquismo14. Teniendo en cuenta estas referencias, nuestro objetivo fue analizar la asociación entre la LTLa, las variables bioquímico - clínicas y los componentes del SM, dado que el acortamiento de los telómeros es un reflejo del estrés oxidativo crónico al que se ven sometidas las células de los pacientes con el aumento de los factores de riesgo. Encontramos una asociación significativa entre el mayor número de componentes del SM y la menor LTLa (p<0,001; R2 = 0,06, B =-1,275; IC 95% B = -1,926/-0,624). El grupo de individuos sin ningún componente del SM (grupo 0) presentó diferencias en la LTLa con respecto al grupo 1 (p = 0,008), al grupo 2 (p = 0,001) y al grupo SM (p<0,001), con lo cual inferimos que la presencia de al menos uno de los componentes asociados al SM ejerce una influencia negativa sobre la homeostasis de los telómeros. Debido a que el SM, con frecuencia, progresa y culmina en el desarrollo de la DT2, el objetivo siguiente fue analizar la LTLa en pacientes con DT2 de reciente diagnóstico, a través de un estudio prospectivo controlado, para ver su posible acción sobre el acortamiento telomérico observado en dichos pacientes. En 2005, se estableció la asociación entre LT en células blancas circulantes y la presencia de DT251; en ella la LT en leucocitos de pacientes diabéticos es significativamente menor que en los controles sanos, en parte por la mayor susceptibilidad al daño oxidativo del ADN en estos pacientes45.
Por otro lado, un estudio mostró una disminución del 50 % en el SM y la DT2 con solo 3 semanas de un tratamiento que consistió en una intensa modificación del estilo de vida mediante dieta y actividad física52. De acuerdo con lo comentado, pensamos que la mejora en alguno de los componentes del SM a través de tratamientos farmacológicos o medidas higiénico - dietéticas, que mejoran la compensación metabólica de los pacientes, se puede ver reflejada en la LTLa.
Los resultados de este estudio indican que los 30 pacientes pudieron ser compensados metabólicamente, lo que resultó en una disminución estadísticamente significativa en los valores de HbA1c (p < 0,001) y glucemia (p = 0,001) entre los grupos pre y pos-intervención. Al evaluar comparativamente la LTLa entre los individuos en los diferentes momentos del estudio, observamos un comportamiento aleatorio de la LTLa, que no se asoció a ninguna variable bioquímico - clínica ni a la compensación metabólica evaluada por glucemia y HbA1c ni al tiempo de tratamiento. En un trabajo reciente de seguimiento a 6 años, fueron estudiados 3.600 pacientes, de los cuales el 44 % presentó un acortamiento en la LTLa; en el 22 %, esta se mantuvo estable y se alargó en el 34 % de los individuos estudiados53-54. Nuestros datos también apoyan la noción de un patrón dinámico que incluye acortamiento y alargamiento de la LT a lo largo del tiempo. El mecanismo para esta LT oscilante de la reserva de leucocitos en circulación no está claro, pero puede deberse a diferencias en las fracciones celulares o a verdaderos efectos biológicos, tales como la activación de la telomerasa transitoria55,56. Por otro lado, uno de los principales hallazgos de nuestro estudio fue la asociación positiva, significativa entre la variación de la LTLa, luego del tratamiento, y la dosis de metformina empleada (p = 0,007). Hay evidencia de que el uso de metformina, que es la principal droga utilizada para el tratamiento de la DT2, está relacionada con la disminución del estrés oxidativo en la célula, demostrado por la disminución en la concentración de las especies reactivas del oxígeno ROS57, con lo cual, concluimos que la metformina podría tener un efecto positivo en los pacientes con DT2, que puede trasladarse a los telómeros. Se puede decir que nuestros resultados apoyan las evidencias de la metformina como fármaco con características geroterapéuticas debido a su acción antiinflamatoria directa, más allá de ser un agente hipoglucemiante58,59.
Por último, se observó que la longitud de los telómeros aumenta en los pacientes sometidos a cirugía bariátrica, lo cual se debe, probablemente, al mejoramiento del estado metabólico y la disminución del estado de inflamación. Al estudiar si una disminución significativa de los niveles de inflamación podría mejorar la LTa, subdividiendo a los pacientes en obesos y obesos mórbidos, observamos que los pacientes obesos mórbidos, a los 6 meses de la cirugía, presentaron un aumento significativo de la LTa y una disminución significativa de los niveles de inflamación, mientras que los pacientes obesos no presentaron cambios.
Se concluye que, aunque los mecanismos que subyacen al desarrollo del SM son complejos, el estrés oxidativo y la inflamación pueden desempeñar un papel crucial en este proceso y podrían contribuir al acortamiento acelerado de los telómeros. En este trabajo, pudimos evidenciar que la presencia de uno o más factores de riesgo característicos del SM se asocian con una menor LTLa, la cual es todavía menor en el grupo de pacientes con SM. En este sentido, cabe destacar la importancia de contar con una adecuada identificación clínica, bioquímica y genético - molecular en los individuos OMS o incluso en los individuos sanos, donde la longitud telomérica alterada para su edad se constituiría en un buen marcador del estado metabólico y serviría para individualizar pacientes a intervenir en forma temprana. A través de los resultados del presente trabajo, se contribuye al conocimiento de las bases moleculares que definen una forma de presentación clínica o fenotipo específico de obesidad, como es la que se presenta en individuos obesos sin el desarrollo de las alteraciones metabólicas características del SM, los denominados obesos metabólicamente sanos. En ese sentido, medidas de intervención como la cirugía bariátrica, de alto costo para el sistema de salud, que tiene un impacto relevante en la obesidad mórbida y en obesos con SM, podrían ser replanteadas para pacientes OMS, los que presentan una menor evolución hacia la diabetes tipo 2 y la enfermedad cardiovascular. Así se produce una contribución concreta al sistema de salud, ya que este fenotipo de obesidad no se estaría beneficiando con una intervención tan compleja y costosa y se vería beneficiado con medidas de intervención más simples en cuanto al estilo de vida como la dietoterapia y la actividad física.
Por otro lado, la LTLa debe ser entendida como una variable dinámica, que depende, entre otras cosas, de las condiciones del estilo de vida y del estado metabólico, y que, particularmente a través de los estudios de intervención, redundaría en beneficios más sostenibles a mediano y largo plazo no solo en el nivel de las características antropométricas de los pacientes afectados, sino también en el estado de inflamación subclínica, con la consecuente disminución del estrés oxidativo, reflejado, en este caso, en un aumento del tamaño telomérico. Se desprende la necesidad de mantener un adecuado control, dentro de las metas establecidas, de los diferentes parámetros metabólicos (lípidos, glucemia, estado oxidativo, inflamación, etc.) mediante diferentes medidas de intervención, ya sea con cambios en el estilo de vida o con drogas, más allá del peso, para mejorar el impacto en la función celular, del cual el telómero se constituye en un marcador fundamental.
Los hallazgos obtenidos a partir de este trabajo podrían influir positivamente en la predicción, prevención y el tratamiento de la obesidad y diabetes. Las medidas de intervención que tengan en cuenta los factores inflamatorios, de estrés oxidativo e IR y, en un futuro cercano, las intervenciones de tipo farmacológico personalizado a partir de la caracterización genética – epigenética - marcadores de inflamación y de respuesta al ambiente de cada paciente impactarán claramente en el diagnóstico y pronóstico del individuo con obesidad y las alteraciones metabólicas asociadas.
Referencias bibliográficas
1. Blackburn EH. Telomeres: no end in sight. Cell. 1994;77(5):621-3.
2. Meyne J, Ratliff RL, Moyzis RK. Conservation of the human telomere sequence (TTAGGG)n among vertebrates. Proc Natl Acad Sci U S A. 1989;86(18):7049-53.
3. Makarov VL, Hirose Y, Langmore JP. Long G tails at both ends of human chromosomes suggest a C strand degradation mechanism for telomere shortening. Cell. 1997;88(5):657-66.
4. Wright WE, Tesmer VM, Huffman KE, Levene SD, Shay JW. Normal human chromosomes have long G-rich telomeric overhangs at one end. Genes Dev. 1997;11(21):2801-9.
5. Griffith JD, Comeau L, Rosenfield S, Stansel RM, Bianchi A, Moss H, et al. Mammalian telomeres end in a large duplex loop. Cell. 1999;97(4):503-14.
6. Blackburn EH. Telomere states and cell fates. Nature. 2000;408(6808):53-6.
7. Olovnikov AM. A theory of marginotomy. The incomplete copying of template margin in enzymic synthesis of polynucleotides and biological significance of the phenomenon. J Theor Biol. 1973;41(1):181-90.
8. Watson JD. Origin of concatemeric T7 DNA. Nat New Biol. 1972;239(94):197-201.
9. Mikhelson VM, Gamaley IA. Telomere shortening is a sole mechanism of aging in mammals. Curr Aging Sci. 2012;5(3):203-8.
10. von Zglinicki T, Martin-Ruiz CM. Telomeres as biomarkers for ageing and age-related diseases. Curr Mol Med. 2005;5(2):197-203.
11. Révész D, Milaneschi Y, Verhoeven JE, Penninx BW. Telomere length as a marker of cellular aging is associated with prevalence and progression of metabolic syndrome. J Clin Endocrinol Metab. 2014;99(12):4607-15.
12. Rode L, Nordestgaard BG, Bojesen SE. Peripheral blood leukocyte telomere length and mortality among 64,637 individuals from the general population. J Natl Cancer Inst. 2015;107(6):djv074.
13. Epel ES, Blackburn EH, Lin J, Dhabhar FS, Adler NE, Morrow JD, et al. Accelerated telomere shortening in response to life stress. Proc Natl Acad Sci U S A. 2004;101(49):17312-5.
14. Valdes AM, Andrew T, Gardner JP, Kimura M, Oelsner E, Cherkas LF, et al. Obesity, cigarette smoking, and telomere length in women. Lancet. 2005;366(9486):662-4.
15. Petersen S, Saretzki G, von Zglinicki T. Preferential accumulation of single-stranded regions in telomeres of human fibroblasts. Exp Cell Res. 1998;239(1):152-60.
16. Oikawa S, Kawanishi S. Site-specific DNA damage at GGG sequence by oxidative stress may accelerate telomere shortening. FEBS Lett. 1999;453(3):365-8.
17. Kawanishi S, Oikawa S. Mechanism of telomere shortening by oxidative stress. Ann N Y Acad Sci. 2004;1019:278-84.
18. O'Donovan A, Pantell MS, Puterman E, Dhabhar FS, Blackburn EH, Yaffe K, et al. Cumulative inflammatory load is associated with short leukocyte telomere length in the Health, Aging and Body Composition Study. PLoS One. 2011;6(5):e19687.
19. Lumeng CN, Saltiel AR. Inflammatory links between obesity and metabolic disease. J Clin Invest. 2011;121(6):2111-7.
20. Grundy SM, Cleeman JI, Daniels SR, Donato KA, Eckel RH, Franklin BA, et al. Diagnosis and management of the metabolic syndrome: an American Heart Association/National Heart, Lung, and Blood Institute Scientific Statement. Circulation. 2005;112(17):2735-52.
21. Gallagher EJ, LeRoith D, Karnieli E. The metabolic syndrome--from insulin resistance to obesity and diabetes. Endocrinol Metab Clin North Am. 2008;37(3):559-79, vii.
22. Grundy SM. Obesity, metabolic syndrome, and cardiovascular disease. J Clin Endocrinol Metab. 2004;89(6):2595-600..
23. Obesidad y sobrepeso [Internet]. www.who.int. Available from: http://www.who.int/mediacentre/factsheets/fs311/es/
24. Encuesta Nacional 4° de Factores de Riesgo Principales resultados. [Internet]. Available from: https://bancos.salud.gob.ar/sites/default/files/2020-01/4ta-encuesta-nacional-factores-riesgo_2019_principales-resultados.pdf
25. Arteaga A. El sobrepeso y la obesidad como un problema de salud. Revista Médica Clínica Las Condes. 2012;23(2):145–53.
26. de Sereday MS, Gonzalez C, Giorgini D, De Loredo L, Braguinsky J, Cobeñas C, et al. Prevalence of diabetes, obesity, hypertension and hyperlipidemia in the central area of Argentina. Diabetes Metab. 2004;30(4):335-9.
27. Schargrodsky H, Hernández-Hernández R, Champagne BM, Silva H, Vinueza R, Silva Ayçaguer LC, et al; CARMELA Study Investigators. CARMELA: assessment of cardiovascular risk in seven Latin American cities. Am J Med. 2008;121(1):58-65.
28. Fiorentino TV, Prioletta A, Zuo P, Folli F. Hyperglycemia-induced oxidative stress and its role in diabetes mellitus related cardiovascular diseases. Curr Pharm Des. 2013;19(32):5695-703.
29. Green K, Brand MD, Murphy MP. Prevention of mitochondrial oxidative damage as a therapeutic strategy in diabetes. Diabetes. 2004;53 Suppl 1:S110-8.
30. Dudinskaya EN, Tkacheva ON, Shestakova MV, Brailova NV, Strazhesko ID, Akasheva DU, et al. Short telomere length is associated with arterial aging in patients with type 2 diabetes mellitus. Endocr Connect. 2015;4(3):136-43.
31. Gardner JP, Li S, Srinivasan SR, Chen W, Kimura M, Lu X, et al. Rise in insulin resistance is associated with escalated telomere attrition. Circulation. 2005;111(17):2171-7.
32. Murillo-Ortiz B, Albarrán-Tamayo F, Arenas-Aranda D, Benítez-Bribiesca L, Malacara-Hernández JM, Martínez-Garza S, et al. Telomere length and type 2 diabetes in males, a premature aging syndrome. Aging Male. 2012;15(1):54-8.
33. Iglesias Molli AE, Panero J, Dos Santos PC, González CD, Vilariño J, Sereday M, et al. Metabolically healthy obese women have longer telomere length than obese women with metabolic syndrome. PLoS One. 2017;12(4):e0174945.
34. National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III). Third Report of the National Cholesterol Education Program (NCEP) Expert Panel on Detection, Evaluation, and Treatment of High Blood Cholesterol in Adults (Adult Treatment Panel III) final report. Circulation. 2002;106(25):3143-421. PMID: 12485966.
35. Alberti KG, Eckel RH, Grundy SM, Zimmet PZ, Cleeman JI, Donato KA, et al. Harmonizing the metabolic syndrome: a joint interim statement of the International Diabetes Federation Task Force on Epidemiology and Prevention; National Heart, Lung, and Blood Institute; American Heart Association; World Heart Federation; International Atherosclerosis Society; and International Association for the Study of Obesity. Circulation. 2009;120(16):1640-5.
36. Murray MG, Thompson WF. Rapid isolation of high molecular weight plant DNA. Nucleic Acids Res. 1980;8(19):4321-5.
37. O'Callaghan NJ, Fenech M. A quantitative PCR method for measuring absolute telomere length. Biol Proced Online. 2011;13:3.
38. Slagboom PE, Droog S, Boomsma DI. Genetic determination of telomere size in humans: a twin study of three age groups. Am J Hum Genet. 1994;55(5):876-82.
39. Tramer F, Caponecchia L, Sgrò P, Martinelli M, Sandri G, Panfili E, et al. Native specific activity of glutathione peroxidase (GPx-1), phospholipid hydroperoxide glutathione peroxidase (PHGPx) and glutathione reductase (GR) does not differ between normo- and hypomotile human sperm samples. Int J Androl. 2004;27(2):88-93.
40. Harley CB, Futcher AB, Greider CW. Telomeres shorten during ageing of human fibroblasts. Nature. 1990;345(6274):458-60.
41. Müezzinler A, Zaineddin AK, Brenner H. A systematic review of leukocyte telomere length and age in adults. Ageing Res Rev. 2013;12(2):509-19.
42. Ju Z, Rudolph KL. Telomeres and telomerase in cancer stem cells. Eur J Cancer. 2006;42(9):1197-203.
43. Risques RA, Vaughan TL, Li X, Odze RD, Blount PL, Ayub K, et al. Leukocyte telomere length predicts cancer risk in Barrett's esophagus. Cancer Epidemiol Biomarkers Prev. 2007;16(12):2649-55.
44. Brouilette S, Singh RK, Thompson JR, Goodall AH, Samani NJ. White cell telomere length and risk of premature myocardial infarction. Arterioscler Thromb Vasc Biol. 2003;23(5):842-6.
45. Sampson MJ, Winterbone MS, Hughes JC, Dozio N, Hughes DA. Monocyte telomere shortening and oxidative DNA damage in type 2 diabetes. Diabetes Care. 2006;29(2):283-9.
46. Adaikalakoteswari A, Balasubramanyam M, Ravikumar R, Deepa R, Mohan V. Association of telomere shortening with impaired glucose tolerance and diabetic macroangiopathy. Atherosclerosis. 2007;195(1):83-9.
47. Balasubramanyam M, Adaikalakoteswari A, Monickaraj SF, Mohan V. Telomere shortening & metabolic/vascular diseases. Indian J Med Res. 2007;125(3):441-50. .
48. Mulder H. Is shortening of telomeres the missing link between aging and the Type 2 Diabetes epidemic? Aging (Albany NY). 2010;2(10):634-6.
49. Samani NJ, Boultby R, Butler R, Thompson JR, Goodall AH. Telomere shortening in atherosclerosis. Lancet. 2001;358(9280):472-3.
50. Jeanclos E, Schork NJ, Kyvik KO, Kimura M, Skurnick JH, Aviv A. Telomere length inversely correlates with pulse pressure and is highly familial. Hypertension. 2000;36(2):195-200
51. Adaikalakoteswari A, Balasubramanyam M, Mohan V. Telomere shortening occurs in Asian Indian Type 2 diabetic patients. Diabet Med. 2005;22(9):1151-6.
52. Roberts CK, Won D, Pruthi S, Kurtovic S, Sindhu RK, Vaziri ND, et al. Effect of a short-term diet and exercise intervention on oxidative stress, inflammation, MMP-9, and monocyte chemotactic activity in men with metabolic syndrome factors. J Appl Physiol (1985). 2006;100(5):1657-65.
53. Huzen J, Wong LS, van Veldhuisen DJ, Samani NJ, Zwinderman AH, Codd V, et al. Telomere length loss due to smoking and metabolic traits. J Intern Med. 2014;275(2):155-63.
54. Svenson U, Nordfjäll K, Baird D, Roger L, Osterman P, Hellenius ML, et al. Blood cell telomere length is a dynamic feature. PLoS One. 2011;6(6):e21485.
55. Lin J, Epel E, Cheon J, Kroenke C, Sinclair E, Bigos M, et al. Analyses and comparisons of telomerase activity and telomere length in human T and B cells: insights for epidemiology of telomere maintenance. J Immunol Methods. 2010;352(1-2):71-80.
56. Epel ES, Lin J, Dhabhar FS, Wolkowitz OM, Puterman E, Karan L, et al. Dynamics of telomerase activity in response to acute psychological stress. Brain Behav Immun. 2010;24(4):531-9.
57. de Kreutzenberg SV, Ceolotto G, Cattelan A, Pagnin E, Mazzucato M, Garagnani P, et al. Metformin improves putative longevity effectors in peripheral mononuclear cells from subjects with prediabetes. A randomized controlled trial. Nutr Metab Cardiovasc Dis. 2015;25(7):686-93.
58. Barzilai N, Crandall JP, Kritchevsky SB, Espeland MA. Metformin as a Tool to Target Aging. Cell Metab. 2016;23(6):1060-1065.
59. Saisho Y. Metformin and Inflammation: Its Potential Beyond Glucose-lowering Effect. Endocr Metab Immune Disord Drug Targets. 2015;15(3):196-205.
Figura 1. Longitud telomérica leucocitaria absoluta (LTLa) en función de la edad para la población general. Línea de regresión lineal.

Tabla I. Características bioquímicas, clínicas y antropométricas de la población.
|
Grupos |
NP0 |
OMS |
OSM |
|
|
Media ± DS |
Media ± DS |
Media ± DS |
|
Edad (años) |
36 ± 13a |
42 ± 15b |
51 ± 10c |
|
Peso (Kg) |
62,18 ± 7,98a |
90,05 ± 41,81b |
93,70 ± 17,62b |
|
IMC (Kg m-2) |
22,43 ± 1,72a |
32,70 ± 5,07b |
31,94 ± 5,45b |
|
CC (cm) |
78,13 ± 6,91a |
102,11 ± 12,32b |
107,71 ± 13,33c |
|
HbA1c (%) |
5,4 ± 0,5a |
5,4 ± 0,6a |
5,2 ± 0,3ª |
|
GPA (mg dL-1) |
95 ± 34a |
93 ± 9a |
109 ± 41b |
|
CT (mg dL-1) |
185 ± 42a |
196 ± 35a |
194 ± 34ª |
|
c-HDL (mg dL-1) |
109 ± 32a |
119 ± 27a |
118 ± 31ª |
|
c-LDL (mg dL-1) |
57 ± 13a |
56 ± 13a |
43 ± 9b |
|
TG (mg dL-1) |
89 ± 46a |
96 ± 40a |
180 ± 104b |
NP0, normopeso sin componentes del síndrome metabólico; OM, obeso metabólicamente sano con hasta 2 alteraciones metabólicas del síndrome metabolico; OSM, obeso con síndrome metabólico; IMC, índice de masa corporal; CC, circunferencia de cintura; GPA, glucemia plasmática en ayunas; CT, colesterol total; LDL, colesterol de lipoproteínas de baja densidad; HDL, colesterol de lipoproteínas de alta densidad; TG, triglicéridos; HbA1c, hemoglobina glicosilada. Las variables se presentan como media ± desviación típica (DS) para cada grupo. Los valores de las variables para cada grupo que no comparten el mismo carácter presentan diferencias significativas con una p< 0,05.
Tabla II. Características bioquímicas, clínicas y antropométricas de los grupos pre y posintervención.
|
|
Preintervención |
Posintervención |
|
|
Media ± DS |
Media ± DS |
|
Peso (kg) |
93,25 ± 19,71a |
91,37 ± 19,73b |
|
IMC (kg m-2) |
33,76 ± 5,30a |
33,10 ± 5,33b |
|
CC (cm) |
106,67 ± 15,74a |
104,62 ± 12,74ª |
|
HbA1c (%) |
9,81 ± 1,94a |
6,51 ± 1,01b |
|
GPA (mg dL-1) |
198,16 ± 89,11a |
123,64 ± 45,33b |
|
CT (mg dL-1) |
212,96 ± 74,98a |
207,08 ± 50,46a |
|
c-HDL (mg dL-1) |
40,40 ± 7,08a |
42,32 ± 9,62ª |
|
TG (mg dL-1) |
197,67 ± 129,96a |
213,54 ± 110,00a |
IMC, índice de masa corporal; CC, circunferencia de cintura; GPA, glucemia plasmática en ayunas; CT, colesterol total; LDL, colesterol de lipoproteínas de baja densidad; HDL, colesterol de lipoproteínas de alta densidad; TG, triglicéridos; HbA1c, hemoglobina glicosilada. Los valores de las variables para cada grupo que no comparten el mismo carácter son significativamente diferentes con una p< 0,05. Las variables se presentan como media ± desviación típica (DS) para cada grupo.
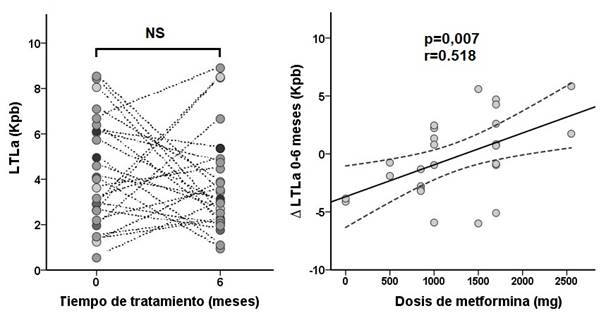 Figura 2. Variación de la
LTLa en función del tiempo de tratamiento y la dosis de metformina.
Figura 2. Variación de la
LTLa en función del tiempo de tratamiento y la dosis de metformina.
Análisis estadístico: comparación de medias por test T para muestras relacionadas; los círculos representan la LTLa de cada individuo a tiempo 0 y 6 meses, unidos mediante líneas punteadas. Por regresión lineal, con la media (línea entera) y los intervalos de confianza para la media (línea punteada), se evaluó la asociación entre la variación de la LTLa y la metformina, a los 6 meses de tratamiento, en función de la dosis.
Tabla III. Características bioquímicas, clínicas y antropométricas de los grupos pre y posintervención.
|
|
Preintervención |
Posintervención |
|
|
Media ± DS |
Media ± DS |
|
Peso (kg) |
120,32±22,76a |
88,95 ± 14,86b |
|
IMC (kg m-2) |
42,68 ± 5,26a |
31,66 ± 3,69b |
|
CC (cm) |
125,68 ± 16,17a |
102,26 ± 13,80a |
|
HbA1c (%) |
6,62 ± 1,56a |
5,68 ± 0,72b |
|
GPA (mg dL-1) |
121,06 ± 39,71a |
94,23 ± 45,33b |
|
CT (mg dL-1) |
185,81 ± 32,23a |
182,77 ± 40,37a |
|
c-HDL (mg dL-1) |
47,10 ± 9,41a |
49,93±10,03b |
|
c-LDL (mg dL-1) |
99,30 ± 32,43a |
111,43 ± 34,16a |
|
TG (mg dL-1) |
174,36 ± 76,21a |
107,14 ± 41,70b |
|
PCR-us (mg L-1) |
7,14 ± 5,15a |
3,27 ± 4,05b |
Las variables se presentan como media ± desviación típica (DS) para cada grupo. IMC: índice de masa corporal; CC, circunferencia de cintura; GPA, glucemia plasmática en ayunas; CT, colesterol total; LDL, colesterol de lipoproteínas de baja densidad; HDL, colesterol de lipoproteínas de alta densidad; TG, triglicéridos; HbA1c, hemoglobina glicosilada; PCR-us, proteína C reactiva ultrasensible. Los valores de las variables para cada grupo que no comparten el mismo carácter son significativamente diferentes en p< 0,05.
Figura 3. Variación de la LTLa en función de la variación de los niveles de PCR-us.
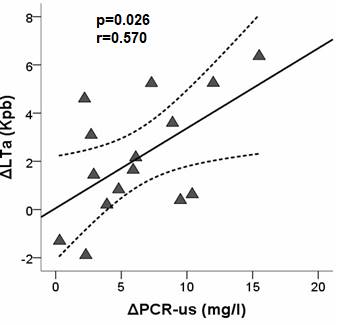
Por regresión lineal, con la media (línea entera) y los intervalos de confianza para la media (línea punteada), se evaluó la asociación entre la variación de la LTLa a los 6 meses de tratamiento en función de la variación de PCR-us. R = coeficiente de correlación de Pearson y significancia con valores de estadístico p<0,05.